応用生物学系 岸川淳一 准教授らの研究グループは、水素イオンの流れを使ってATP合成酵素が回転する仕組みを解明しました
応用生物学系 岸川淳一 准教授らの研究グループは、クライオ電子顕微鏡法(用語1)と分子動力学シミュレーション(用語2)を用いて、好熱菌由来のATP合成酵素(用語3)(用語4)の詳細な構造とその回転メカニズムを明らかにしました。
ATP(アデノシン三リン酸)は、生命にとって最も重要なエネルギー物質であり、細胞のミトコンドリアに存在するATP合成酵素という巨大なタンパク質によって合成されます。この酵素は、生体膜を横断する水素イオンの流れを回転力に変換し、その力でATPを生成します。これまで、水素イオンの流れがどのようにしてATP合成酵素を回転させるのか、その詳細な分子メカニズムは不明でした。しかし、本研究では、ATP合成酵素の回転力を発生させる膜内在部分(Vo部分)の詳細な構造をクライオ電子顕微鏡で解明し、回転力発生に重要な役割を果たすアミノ酸残基の向きを特定しました。さらに、Vo部分の構造を基に分子動力学シミュレーションを行い、水素イオンの流れによる回転メカニズムを解析しました。その結果、回転リングにある特定のアミノ酸残基の荷電状態の変化が回転力発生に重要であることがわかりました。ATP合成酵素は、ヒトから細菌に至る幅広い生物界に存在するタンパク質です。本研究で特定されたアミノ酸残基はすべてのATP合成酵素にほぼ保存されており、この発見は生命がATPを合成する最も重要な仕組みの解明に貢献するものです。
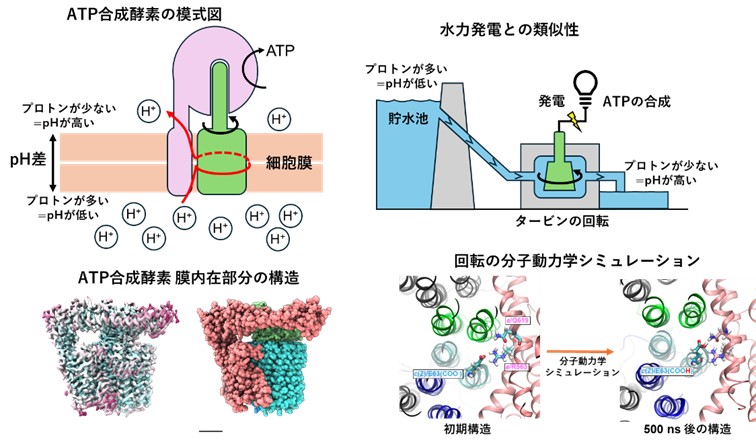
図1.ATP合成酵素の構造解析と分子動力学シミュレーション
本件の詳しい内容はこちら(PDF)
本成果は、2024年11月20日に国際学術誌「Nature Communications」(外部リンク)にオンライン掲載されました。
<用語解説>
1)クライオ電子顕微鏡法 (cryo electron microscopy): 急速凍結したタンパク質などの生体試料に電子線を照射し、試料の観察を行うために透過電子顕微鏡を行う。得られた2次元像から画像解析により、3次元再構成を行い、生体分子の立体構造を決定する。
2)分子動力学シミュレーション (Molecular dynamics simulation): タンパク質の動きを計算する手法の1つ。タンパク質分子を原子レベルでコンピュータの中に再現し、原子間・分子間の相互作用に拘束を与えることで、タンパク質の動きを再現する。シミュレーションの細かさによって、QM/MM、全原子、粗視化などがある。
3)ATP (adenosine triphosphate): 様々な生体反応にエネルギー源として使われるため、細胞のエネルギー通貨とも呼ばれる。ヒトをはじめ多くの生物では、ATP合成のほとんどはATP合成酵素によって担われている。
4)ATP合成酵素 (ATP synthase): ATPの合成を担うタンパク質。真核生物の場合、ミトコンドリア内膜、細菌の場合は細胞膜に存在する。膜に埋まった部分で、生体膜内外に形成されたpH差を回転に変換し、膜から突き出た部分で回転力を使ってATPを合成する(図1)。回転によって反応を行うため、回転分子モーターとも呼ばれる。
【このページに関する問い合わせ先】
総務企画課広報係
TEL:075-724-7016
E-mail:koho[at]jim.kit.ac.jp(※[at]を@に変換してください)
